-
题目: 未知类型
(12分)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) 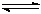
CH3OH(g)。图1表示反应进行过程中能量的变化(曲线a未使用催化剂,曲线b使用催化剂),图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
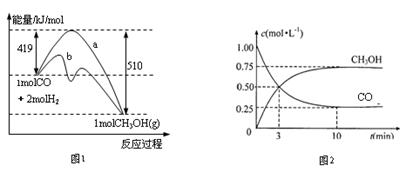
(1)下列说法正确的是______________
(2)从反应开始到平衡状态,用CO浓度变化表示的反应速率为_______________,H2的转化率为______________。A.反应进行到3min时达到化学平衡状态 B.是否使用催化剂对反应前后的能量变化没有影响 C.当反应物消耗量一定时,若反应生成液态甲醇,能量变化值会更大 D.平衡时氢气的浓度为1mol/L (3)当有0.25mol CH3OH生成时会__________(填吸收或放出)___________kJ的热量。
答案不对?请尝试站内搜索
推荐知识点:
- 女,40岁,腹泻1年。体检发现一肛瘘,结肠镜示回盲部铺路石样改变,最可能的诊断是()
- 女婴,胎龄40周出生。出生体重2900g,身长50cm,皮肤红润,胎毛少,足底纹理较多。该新生儿最可能是()
- 当游车起升过高将引绳顶起时,其上开关(二通或过卷阀)打开,连通气路后,经换向阀.快速放汽阀进入刹车气缸,将滚筒刹住。
- 动态报表是指综合反映企业一定时期的经营情况或现金流动情况的报表,( )是动态报表。 A.资产负债表 B.利润表 C.所有者权益变动表 D.现金流量表
- 消防车道的防火巡查要点主要有()
- 患者,女性,62岁,因上腹部不适、疼痛3天,发热38.2℃,以上消化道穿孔,腹膜炎入院。拟急诊行剖腹探查术。患者既往糖尿病史20年,口服降糖药控制血糖。高血压病史3年,口服降压药,血压控制满意。入院后血糖为13.3mmol/L。患者术前可能存在()。
- 下列对Steven-Jonson综合征描述不准确的是()
- 接地装置验收项目().
- 情商的核心内容包括()。
- 下列()房产可以免征房产税。